相转移催化技术具有反应速度快、选择性好、产率高等优点,是一种极具挑战性精细化工和制药工业制备技术。相转移催化已成为有机合成中重要的合成工具。
在有机物和水溶性盐的化学反应中,由于有机物与H2O不互溶,导致反应物之间难以发生有效碰撞,这就使得这类有机反应速率缓慢,甚至不能进行。研究发现,有一类物质可以帮助水溶性盐从水相转移到有机相中,提高反应物分子间的有效碰撞概率,起到催化化学反应进行的作用,这类物质因而得名为相转移催化剂(PTC,Phase Transfer Catalyst)。
相转移催化剂作用原理
相转移催化剂(Phase transfer catalyst,PTC)是可以帮助反应物从一相转移到能够发生反应的另一相当中,从而加快异相系统反应速率的一类催化剂。一般存在相转移催化的反应,都存在水溶液和有机溶剂两相,离子型反应物往往可溶于水相,不溶于有机相,而有机底物则可溶于有机溶剂之中。不存在相转移催化剂时,两相相互隔离,几个反应物无法接触,反应进行得很慢。相转移催化剂的存在,可以与水相中的离子所结合(通常情况),并利用自身对有机溶剂的亲和性,将水相中的反应物转移到有机相中,促使反应发生。
PTC催化原理
季铵盐和冠醚是两类常见的PTC,图1左图所示的是一种常见的季铵盐类PTC——四丁基氯化铵[(CH3CH2CH2CH2)4N]Cl,右图所示的二环己烷基-18-冠-6-醚是一种冠醚类PTC。
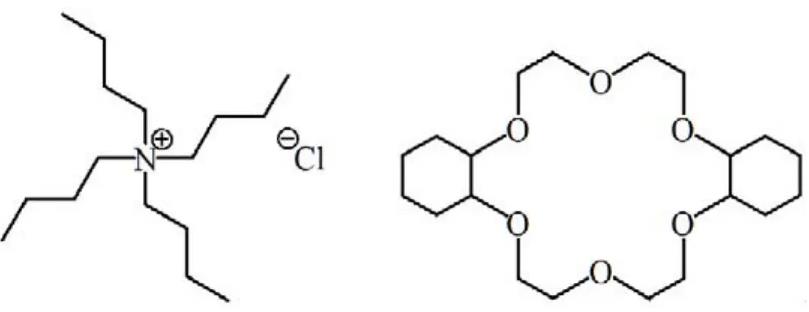
图1四丁基氯化铵(左)和二环己烷-18-冠-6-醚(右)
在此以四丁基氯化铵为例说明PTC的催化原理。如图2所示,两种反应物,即易溶于H2O的反应物Y-和有机物RX,原本分别处于水相和有机相中,反应进行缓慢。作为PTC的[(CH3CH2CH2CH2)4N]Cl(下文用Q+X-表示)能电离出阳离子[(CH3CH2CH2CH2)4N]+(下文用Q+表示)。Q+作为一种阳离子,它可以溶于H2O,而它还含有亲油基团四丁基,因此它也可溶于有机物。因而,Q+具有在H2O和有机物中迁移的能力。Q+遇到H2O中的水溶性盐反应物时,Q+会与水溶性盐的阴离子Y-结合形成离子对Q+Y-,进入有机溶液。Y-在有机溶液中被释放出来,并与有机反应物RX发生化学反应,生成产物RY。释放出来的Q+和Y-结合成PTC分子Q+X-。Q+X-再穿过界面,回到水中,结合下一个水溶性盐反应物的Y-,使催化反应继续进行。
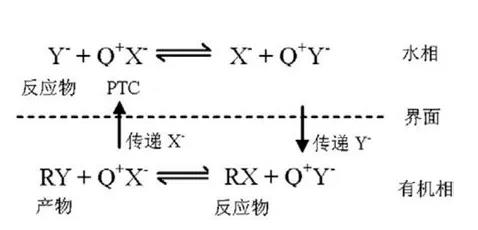
图2 PTC催化原理示意图
一个好的PTC需要具备以下几个结构特点:第一,本身含有Q+或可以形成Q+,以便和H2O中的阴离子Y-形成离子对;第二,分子中应含有足够多的亲油基团,这样形成的离子对Q+Y-才可在有机物中有较好的溶解性;第三,离子对之间的离子键强度要适中,既要保证能将Y-带入有机物中,又要保证在有机物中可以解离出Y-,让其参加反应,这样的PTC才具有反应活性。
相转移催化剂的种类
常用相转移催化剂包括环状冠醚类、聚醚类、季膦盐类以及季铵盐类等,除此外,还有鏻盐、N—烷基膦酰胺、次甲基桥磷或氧硫化合物。
从细分产品来看,传统冠醚类、季铵盐类相转移催化剂存在低毒性、热稳定性差、生产成本高等问题。杂多酸(HPA)作为新型绿色相转移催化剂,具有无毒、氧化还原性及催化活性极强等优势,为目前我国相转移催化剂研究热点之一。